
编者按
自闭症谱系障碍(ASD)是一种复杂的神经发育综合征,其核心表现为社交沟通障碍、重复刻板行为和狭隘兴趣。研究表明,其成因涉及遗传因素(如基因突变)、孕期环境(如感染、毒素暴露)及菌-肠-脑轴功能紊乱等。
今天,我们分享2025年4月29日发表在Scientific Reports上的题为“Seizure-like behavior and hyperactivity in napb knockout zebrafish as a model for autism and epilepsy”的最新研究成果。该研究利用基因编辑技术构建了斑马鱼自闭症及癫痫模型,确定了NAPB基因是自闭症及癫痫的潜在危险基因。
研究发现,敲除NAPB基因的斑马鱼运动神经元轴突长度缩短,并表现出过度活跃的行为异常,如总移动距离、游泳速度、旋转频率增加等,有效模拟了人类癫痫表型。通过结合行为学测试、电生理MEA分析表明,该斑马鱼模型可用于研究自闭症谱系障碍(ASD)和癫痫的病理生理机制,并为相关疾病的药物筛选提供了新工具。
文章题目
Seizure-like behavior and hyperactivity in napb knockout zebrafish as a model for autism and epilepsy
杂志:Scientific Reports(Nature子刊)
发表时间:2025年4月29日
作者:Kyung Chul Shin, Sahar I. Da’as & Yongsoo Park等
单位:卡塔尔哈马德·本·哈利法大学(Hamad Bin Khalifa University, HBKU),卡塔尔生物医学研究所等
01、研究亮点
利用基因编辑技术构建了敲除NAPB基因的斑马鱼自闭症及癫痫模型,发现NAPB功能缺失导致斑马鱼运动神经元发育异常及癫痫样行为;
• 结合行为学、电生理学(MEA)和分子生物学技术,全面解析了癫痫表型的神经机制,揭示了NAPB敲除通过增强大脑区域神经兴奋性,而非突触传递缺陷,诱发癫痫表型;
• NAPB基因敲除的斑马鱼成功模拟了ASD和癫痫的共病表型,如过度活跃、神经超兴奋性等,为病理机制研究提供了新工具,也可用于高通量筛选靶向神经超兴奋性的抗癫痫药物。
02、研究背景
自闭症谱系障碍(ASD)是一种复杂的神经发育综合征,主要表现为重复性行为和社交沟通障碍等。共病现象在ASD患者身上十分普遍,且常伴随多个,其中癫痫是常见症状之一。我们的研究已证实,NAPB(N-乙基马来酰亚胺敏感因子附着蛋白β)是ASD的潜在风险基因。一组卡塔尔ASD三胞胎患者被发现基因杂合突变,其从父母遗传的NAPB纯合基因变异,以致于这三个男孩均表现出不同程度的早期癫痫性脑病,且病情程度和药物反应各异。
基于此,研究人员构建了患者特异性、父母特异性及经过基因修正的NAPB多能干细胞系,这些干细胞分化的人类神经元显示,患者神经元中NAPB功能缺失。此外,两项国际独立研究也发现了两种与癫痫相关的NAPB功能缺失突变,进一步证实了NAPB突变在ASD和癫痫中的关键作用。
NAP,又称可溶性NSF附着蛋白(SNAP),是NSF ATP酶的重要辅助因子,可促进SNARE复合体的解聚,从而释放游离SNARE蛋白以用于后续膜融合反应。NAP-α(NAPA)与NAP-β(NAPB)的序列相似性达83%,分子量分别为33 kDa和34kDa。NAPB在大脑中特异性表达,而NAPA则广泛分布于多种组织。与NAPB基因突变患者的癫痫表型一致,NAPB基因敲除(KO)后的小鼠在出生后表现出严重的复发性癫痫。然而,NAPB基因缺失并不影响细胞水平的突触传递和短期可塑性。同样,在NAPB基因突变的多能干细胞分化的人源皮质神经元中,也未观察到神经元活动及钙内流缺陷,这表明细胞模型可能无法充分模拟癫痫表型。开发NAPB基因突变的动物模型,对研究ASD和癫痫病理机制仍然具有挑战性。
斑马鱼,因其与人类的遗传相似性高、通体透明、明确的中枢神经系统等,被广泛用于癫痫和神经发育障碍研究。斑马鱼的可量化行为,可有效模拟癫痫发作、多动和其他神经发育异常等,为相关疾病建模提供了理想平台。本研究利用基因编辑技术,对两种NAPB直系同源基因——napba、napbb,构建了NAPB斑马鱼模型,以探究NAPB基因相关的癫痫病理机制。
本研究通过构建敲除NAPB基因的斑马鱼,探究其癫痫样表型及NAPB基因遗传变异相关的神经病理特征,并结合行为学测试、MEA电生理功能分析,研究癫痫及相关神经疾病的病理生理机制,揭示NAPB突变如何通过神经超兴奋性诱发疾病表型。
03、研究结果
1. 斑马鱼模型探究NAPB基因突变与癫痫的关联
通过对卡塔尔100多个自闭症家庭进行全外显子组基因测序,证实NAPB基因是自闭症谱系障碍(ASD)和其他神经发育障碍的潜在风险基因。
研究人员通过基因编辑技术,敲除两个napb直系同源基因,构建了NAPB基因敲除斑马鱼(CR),并通过活体成像发现,与对照组相比,NAPB基因敲除的斑马鱼运动神经元轴突长度显著缩短(图1A-B),表明神经发育与连接异常可能引起疾病发生,但神经肌肉突触在轴突分支模式上与对照组无明显差异,表明NAPB缺失可能不直接影响突触结构。
在斑马鱼癫痫模型中,NAPB基因敲除的斑马鱼总移动距离、游泳速度、旋转频率等均显著升高(图1C-E),其行为学变化有效模拟了人类癫痫表型,表明该模型可用于ASD相关癫痫的病理机制研究。
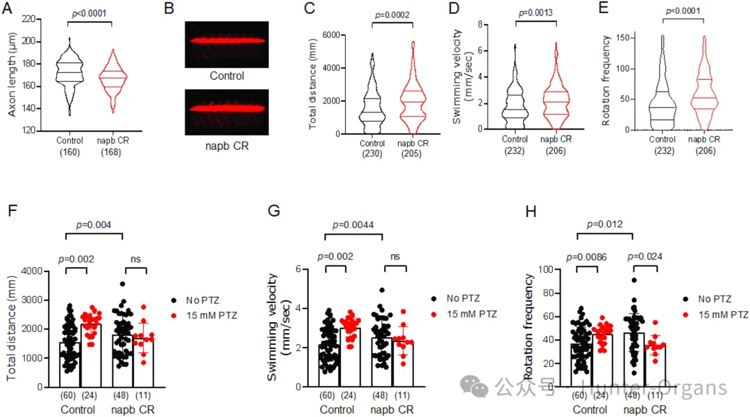
图1
2. PTZ诱导斑马鱼癫痫样活动,但在NAPB敲除的斑马鱼中效果减弱
戊四氮(PTZ)是γ氨基丁酸(GABA-A)及其受体复合物的抑制剂,可用于诱发癫痫、惊厥等。通过降低GABAA的抑制性效应,从而增强神经元兴奋性并诱导斑马鱼癫痫样行为,其常可用于诱导过度活跃及癫痫样运动表型。
研究人员通过定量逆转录PCR(qPCR)分析,发现对照组的斑马鱼表现出显著的行为异常,如总移动距离(图1F)、游泳速度(图1G)及旋转频率(图1H)均显著增加,且PTZ处理期间,斑马鱼的行为异常呈持续性。
进一步探究PTZ对NAPB敲除的斑马鱼的作用,结果显示,在PTZ暴露的前8分钟,NAPB敲除的斑马鱼总移动距离、游泳速度及旋转频率均显著高于对照组;但随着时间的推移,PTZ的效应逐渐减弱,这可能与后续出现的活动停滞期有关。
3. NAPB敲除的斑马鱼神经超活跃与超兴奋性
随后,研究人员利用微电极阵列(MEA)技术来研究斑马鱼的神经活动及神经网络的形成。在对照组斑马鱼中,大脑神经活动(红色信号)与脊髓活动高度同步(图2C),表明其神经系统网络连接完整,大脑激活可触发脊髓及运动神经元的协同放电。相比之下,NAPB敲除的斑马鱼表现出显著的脑区神经超活跃(图2D-F),且脑区异常活跃的个体数量显著高于对照组(图2G)。因此,NAPB敲除的斑马鱼脑部神经超活跃与其癫痫样行为(图1C-E)直接相关,证实了该模型的癫痫表型。
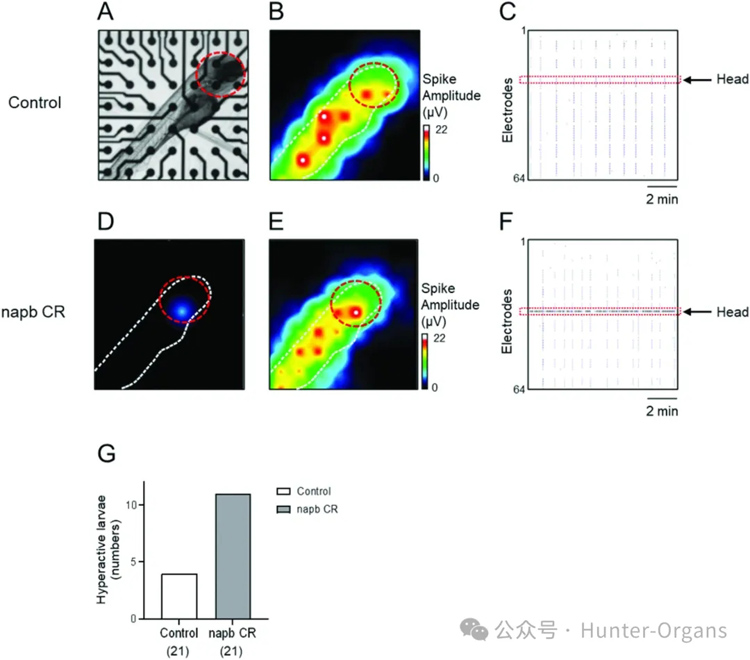
图2
此外,由于NAPB敲除的斑马鱼已处于高神经兴奋状态,在PTZ诱导的癫痫模型中,其超活跃性有所降低,这与NAPB模型先前观察到的癫痫样行为表型一致。
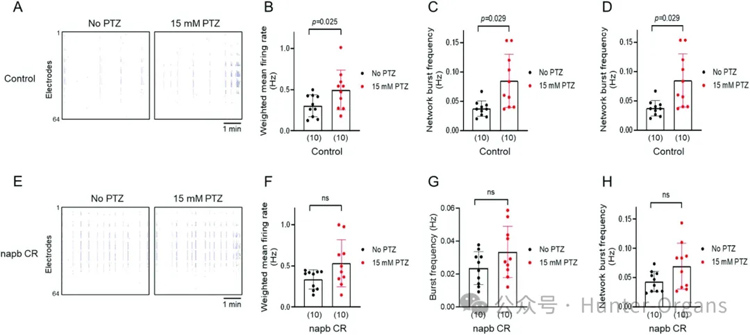
图3
04、编者点评
本研究构建了NAPB敲除的斑马鱼自闭症及癫痫模型,揭示了NAPB功能缺失导致斑马鱼运动神经元发育异常和癫痫样行为,并发现NAPB基因敲除通过增强大脑区域神经兴奋性,而非突触传递缺陷,诱发癫痫表型,为研究ASD和癫痫的病理机制及药物筛选提供了新工具。
作为健康美丽产业CRO服务开拓者与引领者、斑马鱼生物技术的全球领导者,环特生物搭建了“斑马鱼、类器官、哺乳动物、人体”多维生物技术服务体系,开展健康美丽CRO服务、科研服务、智慧实验室搭建三大业务。目前,环特已建立200多种斑马鱼模型,胃癌、脑类器官、心脏类器官及各种肿瘤类器官培养平台,欢迎有需要的读者垂询!
